ЭНЕРГЕТИЧЕСКИЕ МЕТОДОЛОГИИ СТРУКТУРНЫХ ВЗАИМОДЕЙСТВИЙ В ФИЗИКО-ХИМИИ
ЭНЕРГЕТИЧЕСКИЕ МЕТОДОЛОГИИ СТРУКТУРНЫХ ВЗАИМОДЕЙСТВИЙ В ФИЗИКО-ХИМИИ
Аннотация
Энторопийные принципы дают базисную основу формирования функциональных связей между многими величинами химической кинетики. Равновесная сумма энтропийных составляющих универсальной газовой постоянной, равная R/2, имеет прямую математическую связь с тангенсом геодезического угла. Аналогичное соотношение этого параметра получено по графикам Аррениуса – зависимости коэффициента скорости реакции от температуры. При движении в одном формате двух энтропийных составляющих равновесная сумма их энергий равна половине первоначальной величины энергии. Установленные принципы проявляются и в других закономерностях химической кинетике и физике, например, в энергии активации диффузионных процессов и в уравнении кинетической энергии.
1. Введение
Известно , , что понятие энтропии, вытекающее из второго закона термодинамики, является критерием направленности процесса в системе и степенью упорядоченности самой системы молекул или атомов. Если в этих системах их взаимодействие идет по направлению градиента потенциала – положительная работа, то результирующая потенциальная энергия и приведенная масса находятся по принципу сложения обратных величин соответствующих значений (величин подсистем). Такой процесс является корпускулярным, теоретической концепцией которого и являться энтропия. С другой стороны – в системах, в которых взаимодействие идет против градиента потенциала – отрицательная работа, выполняется алгебраическое сложение их масс и энергий, что характеризуется волновым процессом, теоретической концепцией которого может являться негэнтропия. Резонансное стационарное состояние в системе достигается при условии равенства этих энтропийных составляющих – энтропия полностью компенсируется негэнтропией .
Цель работы – установить функциональные количественные связи между энтропией и энергетическими величинами структурных взаимодействий в физико-химии.
2. Энтропия и универсальная газовая постоянная
Газовую постоянную называют универсальной по ее многоплановому применению в химической кинетике и физике. Так, по уравнению состояния газа универсальная газовая постоянная R равна работе расширения 1 моля газа при увеличении температуры на 1⁰ K. А в химической реакции R равна разности молекулярных теплоемкостей при постоянном давлении и объеме газа.
По уравнению Больцмана:
где S – энтропия, k – постоянная Больцмана, w – число доступных состояний.
Заменяя lnw на число Авогадро (А) получаем:
Исходя из уравнения (2), газовую постоянную R можно рассматривать как параметр энтропии, имеющий максимальное значение для любого процесса или системы взаимодействующих молекул или атомов.
В общем случае при поступательном движении системы из двух одинаковых по величине векторов () с разностью фаз 90° их равнодействующая определиться:
Если происходит вращательное движение или движение по спиральной динамике, то вектор () станет касательным вектором и образует угол вращения, для которого с учетом (2) можно записать:
Подставив в (3) выражение (2) получим:
Если принять угол φ как геодезический угол, равный 54,733°(под этим углом, например, тутовый шелкопряд наматывает нить на основу), то получим tgφ=1.4141, т.е. величину достаточно близкую к величине, полученной по зависимости (4). На основании этого можно записать:
Для уточнения уравнения (7) введем квантовую поправку aо=1,00233:
Таким образом, параметр R∙1/2 есть равновесная энтропийная составляющая равная 50% от максимального значения R, натуральный логарифм которого численно равен тангенсу геодезического угла с учетом квантовой поправки ао.
3. Энтропийные номограммы
В работе для оценки степени структурных взаимодействий предложен обменный гамильтониан, полученный в предположении о прямом перекрывании волновых функций взаимодействующих атомов:
где: – спиновый оператор изотропного обменного взаимодействия для пары атомов, I0 – постоянная обмена, S1 и S2 – интегралы перекрывания волновых функций.
Интегралы перекрывания волновых функций моделируются в работе через величину относительной разности энергетических параметров взаимодействующих атомов – коэффициент α (в %). Данный параметр является прямой характеристикой степени энтропийного равновесия в системе. Покажем это на примере номограммы (рис. 1) – зависимости степени структурных взаимодействий (ρ,%) от коэффициента α (%), полученной в работе для широкого класса структур.
Из номограммы следует, что при изменении α от 0 до 5% условия взаимодействия атомов соответствуют условиям энтропийного состояния, при котором =100% и соответствует неограниченной взаимной растворимости атомов взаимодействующих компонентов в твердом состоянии, т.е. максимальной степени волновой составляющей взаимодействия.
Увеличение значений α (рис.1) характеризует нарастание корпускулярных и электростатических свойств атомов одного химического элемента между собой, что приводит к их ограниченной растворимости в атомах другого химического элемента. Для равновесного энтропийного состояния данной системы можно записать (в линейной интерпретации):
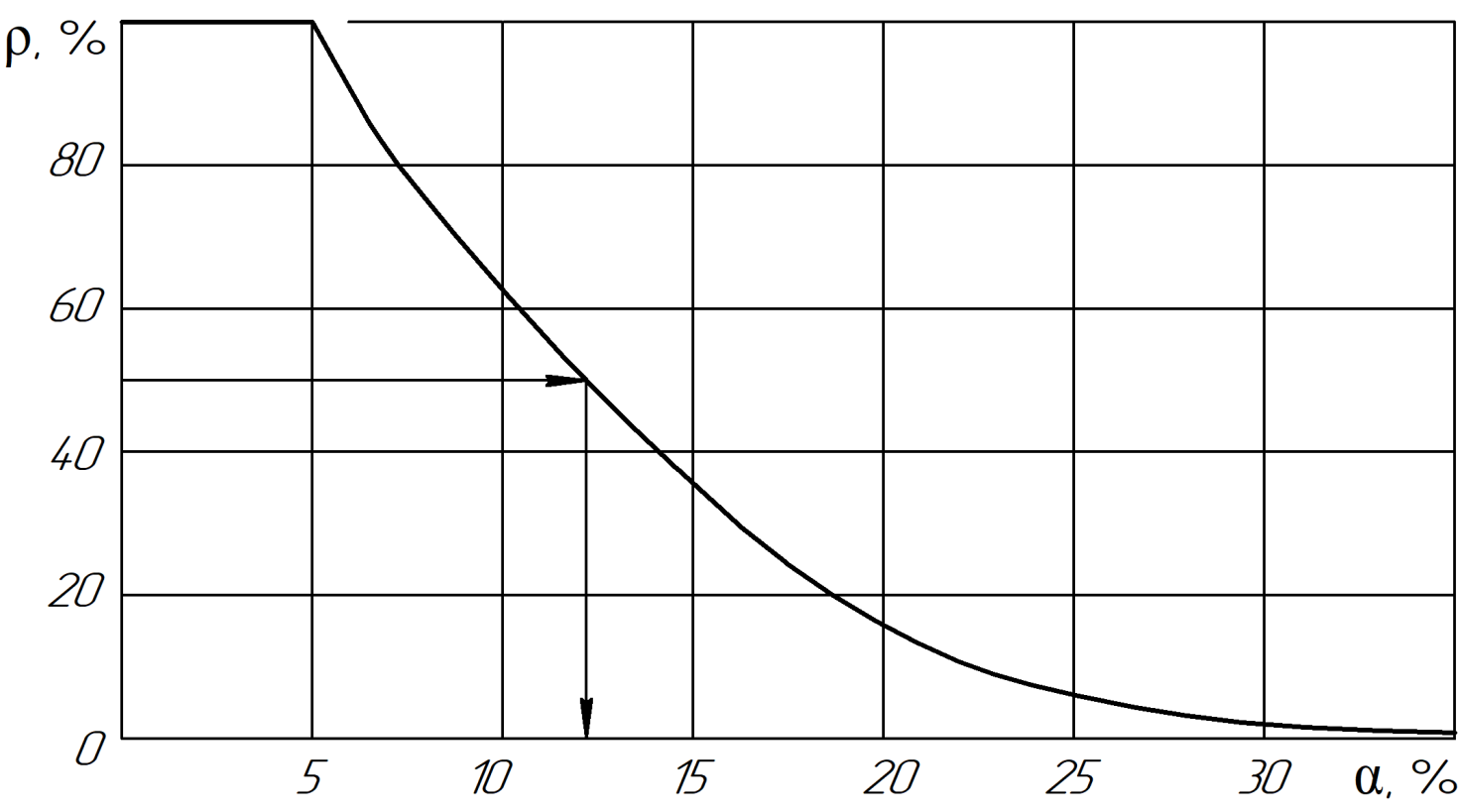
Рисунок 1 - Зависимость степени структурных взаимодействий (ρ) от коэффициента α
4. Энтропия по уравнениям графика Аррениуса
В химической кинетике нередко при исследованиях используются значения средней температуры опыта. Такая методика применяется, например, для оценки энергии активации и предэкспоненциального множителя в уравнении Аррениуса. Можно предположить, что данный подход эквивалентен применению аналогичной величины R∙1/2, определяемой по уравнению (7). Для этого рассмотрим не логарифмический вариант графика зависимости коэффициента скорости химической реакции (Кр) от температуры (Т) (рис. 2).
Данный график аналогичен приведенному выше. В середине графика есть точка, по которой на оси абсцисс есть значение температуры равное примерно 628 К. Она равна среднему значению температуры опыта, то есть 50% от ее максимального значения. На оси ординат ей соответствует значение Кр=17⋅10-4. Значение 50% можно применять в расчётах энтропийных соотношений, но только для негэнтропийной составляющей графика.
Для коэффициента скорости необходимо иметь ее значение в относительных величинах (в процентах). Для этого применим корреляцию коэффициента Кр (по рис.2) со значением a на номограмме (рис.1). По соотношению их максимальных значений, коэффициент корреляции равен 35/50»0.7, поэтому: 17××0.7»11.9a%. Получается уравнение, аналогичное уравнению (5):
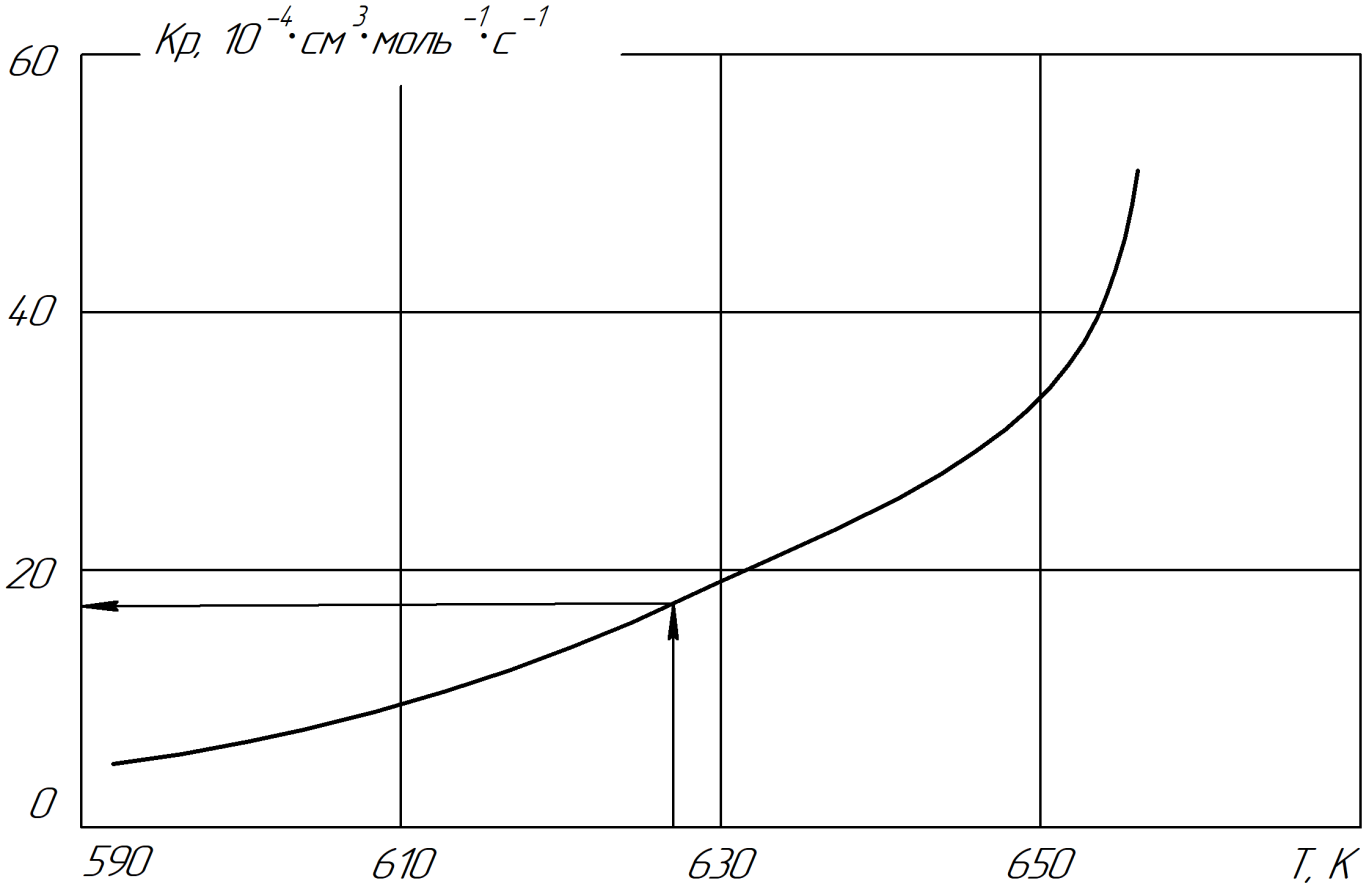
Рисунок 2 - График зависимости коэффициента скорости (К) от температуры (Т)
Примечание: по ист. [4]
5. О факторе электронной концентрации атомов
Известно, что при заданной температуре из двух конкурирующих между собой состояний системы взаимодействующих разнородных атомов устойчиво будет то, которое обладает меньшей свободной энергией . Так энтропия однофазного твердого раствора компонента А в компоненте В (SАВ) всегда выше, чем энтропия SА-В того же сплава, распавшегося на два твердых раствора А и В разной концентрации. Если при этом UАВ < UА-В, то однофазное состояние раствора устойчиво при всех температурах. Если UАВ > UА-В, то при высоких температурах устойчиво состояние двухфазного раствора, а при низких – однофазного. Учитывая взаимодействие между одними лишь ближайшими соседними атомами в кристаллической решетке и не принимая во внимание её упругой деформации, обусловленной различием атомных радиусов химических элементов, условие образования непрерывного ряда твердых растворов выразится :
где UАА, UВВ и UАВ – энергии связи чистых компонентов и их раствора соответственно.
Если 2UАВ > UАА+UВВ, то это означает более сильное взаимодействие между собой одинаковых атомов, чем атомов А с атомами В. Очевидно это связано со строением атомов химических элементов, и в первую очередь с их электронной концентрацией (e/a) – среднее число валентных электронов (e), приходящихся на один атом (a).
Юм-Розери установил, что электронная концентрация однотипных фаз одинакова у всех систем. Так, b – фазы с объемно-центрированной кубической (ОЦК) решеткой и b – фазы с примитивной решеткой (типа CsCl) образуются при электронной концентрации, близкой к 3/2, фазы типа γ-латуни при е/а≈21/13, а ε – фазы с гексагональной плотноупакованной решеткой (ГПУ) – при е/а≈7,4. Объяснение этих особых значений электронной концентрации было дано Джонсом на основе представлений о зонах Бриллюэна. В зоне Бриллюэна имеется место лишь для определенного числа электронов при данном типе структуры. Добавочные электроны могут встроиться в решетку лишь с дополнительной затратой энергии. Вследствие этого более выгодной и более устойчивой окажется новый тип структуры с более высокой предельной концентрацией валентных электронов.
После опубликования работ Юм-Розери и Джонса было найдено, что составы многих металлических фаз обнаруживают, по крайней мере, частичную зависимость от электронной концентрации. Но соотношения между протяженностью твердых растворов и е/а - для них не выполняются. Последнее обстоятельство говорит о том, что фактор электронной концентрации является не единственным и даже не главным фактором фазообразования металлических систем. Данный вывод следует из энтропийных принципов, которые применимы и к атомной структуре. Изначально атом представляет собой систему двух противоположных начал единой действительности. Кинетическая энергия орбитального движения проявляется как негэнтропия, а потенциальная энергия атомного ядра – как энтропия. Энтропийно-равновесное состояние этих составляющих дает стабилизацию атомной структуре в соответствии с уравнением Планка. При этом суммарная энергия атомного центра, рассчитанная по принципу сложения обратных величин исходных составляющих, дает наиболее эффективную энергию каждого атома и может применяться при решении практических задач в материаловедении .
6. Уравнение энергии активации диффузии и самодиффузии
С учетом исходных принципов энтропии, результирующую величину эффективной энергии парного взаимодействия атомов А и В, тождественную энергии активации процесса диффузии, получим в виде суммы обратных величин Р-параметров:
где Еа – энергия активации процесса диффузии атома В среде атомов А; n - число всех валентных электронов, или число наиболее удаленных от ядра валентных электронов конкретного атома.
Цифра 2 в этом уравнении дает среднюю равновесную сумму по каждому атому. Здесь величина , где Рэ – пространственно-энергетический параметр, численно равный эффективной энергии структурных взаимодействий.
Р-параметр был получен в работе путём применения принципов сложения энтропийных составляющих разноименно заряженных систем (принцип сложения обратных величин). В данном случае – это энергия атомного ядра и орбитальная энергия электронов.
При диффузии атома В в однородной по составу и подобной ему среде с атомами В значение Еа приобретает смысл энергии активации самодиффузии атома В. Исходя из (12) она определяется:
Цифру 4 можно рассматривать как произведение двух цифр 2. Одна цифра 2 в знаменателе этого уравнения учитывает среднюю равновесную сумму для каждого атома. Другая цифра 2 – соответствует принципу сложения обратных величин двух одинаковых Р-параметров.
Сопоставление результатов расчетов с экспериментальными данными показало их удовлетворительное совпадение .
Таким образом, во всех рассмотренных примерах равновесная сумма энтропийных составляющих равна половине суммы максимальной первоначальной величины их энергий.
7. Заключение
1. Равновесная сумма энтропийных составляющих универсальной газовой постоянной, равная R/2, имеет прямую математическую связь с тангенсом геодезического угла.
2. Аналогичное соотношение этого параметра получено по графикам Аррениуса – зависимости коэффициента скорости химической реакции от температуры.
3. Установленные принципы проявляются и в других закономерностях физикохимии, например, в энергии активации диффузионных процессов, и могут применяться при решении практических задач в материаловедении.
